LES BIOSIMILAIRES
les BIOSIMILAIRES
En clair, ça veut dire quoi pour moi ?
Un médicament biosimilaire est une copie d’un médicament biologique d’origine dont le brevet est tombé dans le domaine public. Un médicament est dit biologique parce qu’il se compose d’une substance active produite à partir d’une source biologique (cellule, bactérie, levure) ou dérivée de celle-ci.
Le biosimilaire est constitué de la même substance active que le biomédicament d’origine, avec le même dosage et la même forme pharmaceutique.

Comment sont-ils fabriqués ?
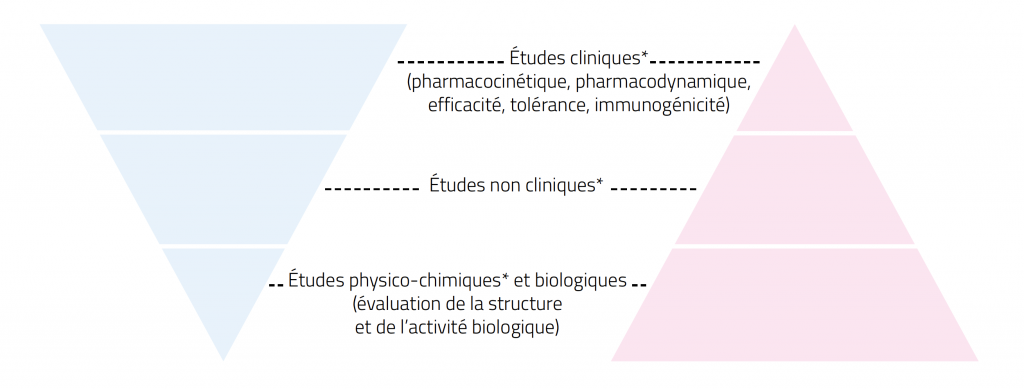
* Pour le médicament biosimilaire, il s’agit d’études comparatives versus le médicament de référence.
(4) European Medecines Agency (EMA) – Biosimilars in the EU – Information guide for healthcare professional 2017.

(3) G. Dranitsaris & K. Dorward & E. Hatzimichael & E. Amir, Clinical trial design in biosimilar drug development, Invest New Drugs (2013) 31: 479–487.
Quelles études pour un biosimilaire ?
Avant l’autorisation de mise sur le marché d’un biosimilaire, différents types d’études sont demandées par l’Agence Européenne du Médicament (EMA) afin de démontrer son équivalence en termes de qualité, d’efficacité et de sécurité par rapport au biomédicament d’origine.
Des études physicochimiques, biologiques, et précliniques démontrent sa biosimilarité au biomédicament d’origine, ainsi que sa qualité.
Puis, des essais cliniques chez l’Homme confirment sa sécurité d’emploi et démontrent son efficacité équivalente au médicament d’origine.
Des études observationnelles post- commercialisation, également appelées « études en vie réelle », peuvent également permettre de confirmer l’efficacité et la tolérance du médicament.
Tous les biomédicaments, y compris les médicaments biosimilaires, suivent les mêmes règles de pharmacovigilance et possèdent un plan de gestion des risques.
LES BIOSIMILAIRES pourquoi y avoir recours ?
La mise à disposition des médicaments biosimilaires a un double intérêt :

SANTÉ PUBLIQUE
en facilitant l’accès aux soins
L’augmentation du nombre de médicaments disponibles permet de limiter les tensions d’approvisionnement et de prévenir les ruptures de stocks et/ou les accidents de production. Le maintien de l’accès à leurs traitements est garanti pour les patients.

ÉCONOMIQUE